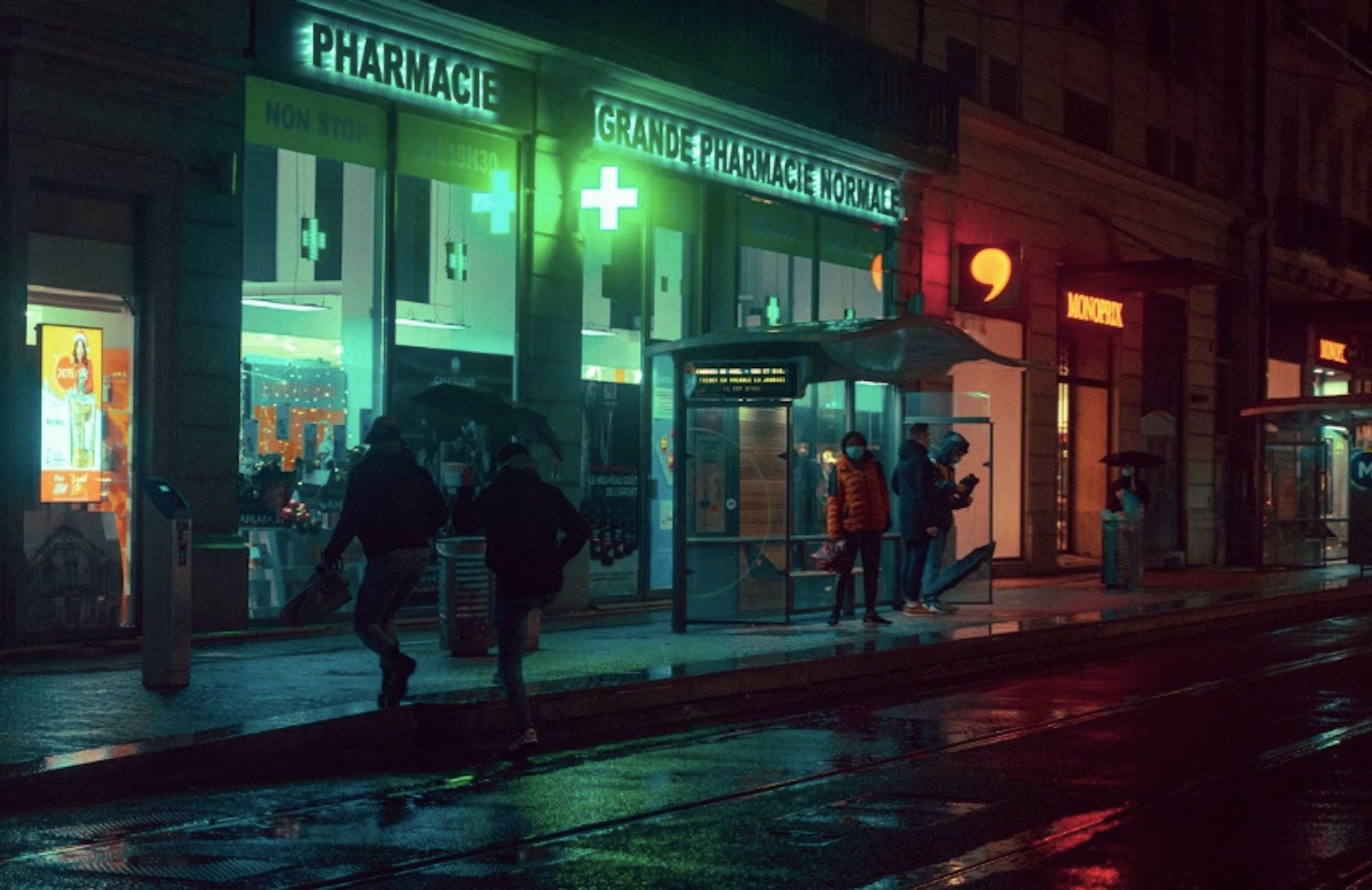Molnupiravir z zielonym światłem od Amerykańskiej Agencji ds. Żywności i Leków
W czwartek kolejna pigułka zwalczająca COVID-19 uzyskała zgodę na dopuszczenie do obrotu leku firmy Merck. Amerykańska Agencja ds. Żywności i Leków (FDA) dzień wcześniej zatwierdziła inną tabletkę zwalczającą koronawirusa.
Molnupiravir z zielonym światłem Amerykańskiej Agencji ds. Żywności i Leków (FDA). Firma Merc uzyskała pozwolenie po Pfizerze.
Tabletka na COVID-19 staje się faktem. Kto będzie mógł korzystać z pigułki firmy Merck i na jakich zasadach odbywać się będzie jej dawkowanie? Okazuje się, że do tego sposobu walki z koronawirusem nie jest potrzebny lekarz.
Pigłuka na COVID-19 z akceptacją FDA
- Dzisiejsze zezwolenie zapewnia dodatkową opcję leczenia wirusa COVID-19 w postaci pigułki, którą można przyjmować doustnie - przekazała w czwartek Patrizia Cavazzoni, dyrektorka Centrum Oceny i Badań Leków FDA.
Dalszy ciąg artykułu pod materiałem wideo
W oficjalnym oświadczeniu podkreśliła, że tabletka przyjmowana doustnie to "przydatna opcja leczenia dla niektórych pacjentów z COVID-19 z wysokim ryzykiem hospitalizacji lub zgonu".
Pojawienie się Omnikronu to zagrożenie, na które tabletka firmy Merck zatwierdzona w czwartek przez FDA ma być częściową odpowiedzią. - Ponieważ wciąż pojawiają się nowe warianty wirusa, kluczowe znaczenie ma rozszerzenie krajowego arsenału terapii COVID-19 z wykorzystaniem autoryzacji do użycia w sytuacjach awaryjnych, przy jednoczesnym dalszym generowaniu dodatkowych danych na temat ich bezpieczeństwa i skuteczności - wyjaśniła Patrizia Cavazzoni.
Tabletkę przyjmujesz w domu
Molnupiravir po zażyciu przez pacjenta ma za zadanie wprowadzić błędy w materiale genetycznym. Ma to utrudnić koronawirusowi replikację.
Doustne zażywanie leku sprawia, że może on być przyjmowany samodzielnie w domu. Fakt ten podkreślono w oświadczeniu na temat dopuszczenia tabletki firmy Merck do obrotu.
Tabletka przeciwko COVID-19 ma być podawana pacjentom poza szpitalem. Osoba przyjmująca lek firmy Merck musi mieć ponad 18 lat. Maksymalny okres przyjmowania pigułki to 5 dni, przy dawkowaniu dwa razy dziennie.
- Molnupiravir nie jest dopuszczony do stosowania u pacjentów w wieku poniżej 18 lat, gdyż może wpływać na wzrost kości i chrząstki - wyjaśniła w czwartkowym oświadczeniu FDA.
- Produkt nie jest dopuszczony do zapobiegania przedekspozycyjnym lub poekspozycyjnym COVID-19 ani do rozpoczynania leczenia u pacjentów hospitalizowanych z powodu COVID-19, ponieważ korzyści z leczenia nie zaobserwowano u osób, które rozpoczęły leczenie po hospitalizacji z powodu COVID- 19 - czytamy w komunikacie prasowym Amerykańskiej Agencji ds. Żywności i Leków.
Co blokuje pojawienie się tabletki przeciwko COVID-19 w Polsce? Na wprowadzenie tego leku do obrotu wydać musi organ analogiczny to FDA: Europejska Agencja Leków (EMA).
Artykuły polecane przez redakcję Goniec.pl:
Prezydent Andrzej Duda podpisał ustawę o modernizacji służb mundurowych
Słowacy drwią z polskich autobusów elektrycznych. W sieci pojawiło się nagranie
"Ziobro jest największym szkodnikiem tego rządu". Radna PiS odchodzi z klubu
Jeżeli chcesz się podzielić informacjami ze swojego regionu, koniecznie napisz do nas na adres [email protected]
Źródło: fda.gov